광화학 [photochemistry, 光化學]
 2016-11-07
2016-11-07
빛에 의한 화학 반응을 연구하는 물리화학의 한 분야. 빛을 흡수한 물질의 화학 반응, 또는 화학 반응의 결과 일어나는 발광 현상(發光現象) 등을 연구하는 학문이다. 전자 상태의 연구와 들뜬 분자의 반응, 발광, 활성 상실 등의 과정 연구도 포함된다.
광화학은 기초적인 분야로서 원자나 분자의 전자 상태, 자유 라디칼의 생성 및 반응, 기본 반응 과정 등의 연구와 밀접한 관계가 있다. 빛에 의해 물질이 변한다는 사실은 햇빛에 의한 물감의 퇴색처럼 예전부터 관찰되고 있었으며, 탄소 동화 작용 등 널리 알려진 것도 많았으나, 광화학의 기초가 확립된 것은 빛의 본질에 대한 인식이 명확해진 20세기에 들어온 후이다. 20세기 초부터 발전한 양자론(量子論)과 이를 기초로 한 원자 · 분자의 규명은 광화학의 이론적 바탕이 되었다. 빛은 광양자(光陽子) 또는 광자(光子)라는 에너지 입자의 흐름이며 빛이 물질에 닿으면 물질 내의 전자가 이 에너지를 얻어 높은 에너지 상태가 된다. 이를 광여기(光勵起)라 한다.
광여기된 물질은 대부분 원상태로 돌아가지만 종류에 따라서는 분해되거나 다른 물질과 화학반응을 일으켜 새로운 물질을 합성한다. 광여기된 원 ·분자의 수명 · 전자구조 · 화학적 성질의 연구에 의해 레이저가 발견되었다. 가장 가까이에서 볼 수 있는 광화학 반응인 사진의 현상(現像)에서는 젤라틴 속에 할로겐화은 결정을 분산시키고, 거기에 빛을 쬐면 빛이 닿은 부분의 할로겐화은이 불안정하게 되므로 여기에 히드로퀴논 · 메롤 둥의 환원제(還元劑)를 작용시켜 은입자(銀粒子)를 석출한다. 실제 사진의 경우에는 빛의 양이 적어도 될 수 있게 빛을 쪼인 할로겐화은을 함유한 결정 전체가 흑화(黑化) 하도록 되어 있다.
광화학의 기본 법칙으로는 제 1법칙과 제 2법칙이 있다. 광화학 제 1법칙은 「물질에 의하여 흡수된 빛만이 광화학 반응을 일으킬 수 있다」는 것이다. 광화학 반응 제 2법칙은 「빛의 흡수는 언제나 광량자(光量子)를 단위로 하여 이루어지며, 흡수는 항상 분자나 원자가 한 번에 단 하나의 광량자를 둘러싸는 꼴로 일어난다」는 것이다. 이 제 2법칙은 아인슈타인의 광량자설에 입각하여 빛을 E=h (h는 플랑크 상수,
(h는 플랑크 상수,  는 빛의 진동수)의 에너지를 가지며, P=h/
는 빛의 진동수)의 에너지를 가지며, P=h/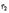 (
(  는 빛의 파장)의 운동량을 가진 하나의 입자(광량자)로 생각하여 분자나 원자가 한 번에 하나의 광량자를 둘러싼다는 것을 의미한다.
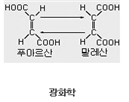
광화학 반응의 예로는 빛이 반응 분자에 대한 활성화 에너지를 부여하므로 자유 에너지가 증가하는 식물의 광합성을 들 수 있다. 또한 사진 화학, 형광, 인광 등의 분야에서도 활용되고 있다.
는 빛의 파장)의 운동량을 가진 하나의 입자(광량자)로 생각하여 분자나 원자가 한 번에 하나의 광량자를 둘러싼다는 것을 의미한다.
광화학 반응의 예로는 빛이 반응 분자에 대한 활성화 에너지를 부여하므로 자유 에너지가 증가하는 식물의 광합성을 들 수 있다. 또한 사진 화학, 형광, 인광 등의 분야에서도 활용되고 있다.


- 다음
- 괴상중합 [bulk polymerization, 塊狀重合] 2016.11.07
- 이전
- 꽃밥(anther) 2016.11.07














![[핫클립] 고차조화파가 어떻게 아토초 펄스를 생성할까](/jnrepo/upload/cmBbs/202405/1b7467a36d0e49ef9a1f50d4caee603f_1716876709887.jpg)
![[핫클립] 단일 아토초 펄스는 어떻게 활용할 수 있을까?](/jnrepo/upload/cmBbs/202405/bc2eaf6109064c0cbf190678e38c1c6c_1716789913738.jpg)

















