깁스-뒤앙의 관계[Gibbs-Duhem relation, -關係]
 2015-12-11
2015-12-11
[요약] 열평형에 있는 다성분계(多成分系)에서 i 성분의 화학 포텐셜을 μi, 농도를 xi라 하고 압력 · 온도를 일정하게 하여 농도를 변화시킬 때 성립되는 Σxidμi=0의 관계. 특히 두 성분일 때는 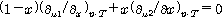 이 된다.
열평형에 있는 다성분계(多成分系)에서 i 성분의 화학 포텐셜을 μi, 농도를 xi라 하고 압력 · 온도를 일정하게 하여 농도를 변화시킬 때 성립되는 Σxidμi=0의 관계. 특히 두 성분일 때는
이 된다.
열평형에 있는 다성분계(多成分系)에서 i 성분의 화학 포텐셜을 μi, 농도를 xi라 하고 압력 · 온도를 일정하게 하여 농도를 변화시킬 때 성립되는 Σxidμi=0의 관계. 특히 두 성분일 때는 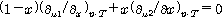 이 된다.
이것은 원래 열역학적 관계식 SdT-Vdp+ΣNidμi=0의 특수한 경우로서 이것 역시 깁스-뒤앙의 관계라고 한다. 이 후자의 관계는 깁스의 자유에너지 G의 변화가 dG=-SdT+Vdp+ΣμidNi이고, G=ΣNiμi이므로 dG=Σ(Nidμi+μidNi)가 주어진다. 따라서 이 양자를 같다고 놓았을 때 얻을 수 있는 관계식이다.
이 된다.
이것은 원래 열역학적 관계식 SdT-Vdp+ΣNidμi=0의 특수한 경우로서 이것 역시 깁스-뒤앙의 관계라고 한다. 이 후자의 관계는 깁스의 자유에너지 G의 변화가 dG=-SdT+Vdp+ΣμidNi이고, G=ΣNiμi이므로 dG=Σ(Nidμi+μidNi)가 주어진다. 따라서 이 양자를 같다고 놓았을 때 얻을 수 있는 관계식이다.
- 다음
- 깔때기[funnel] 2015.12.11
- 이전
- 길만테스트[Gilman test] 2015.12.11













![[핫클립] 집에서 찾는 바닷속 수학](/jnrepo/uploads/2022/04/핫클립-집에서-찾는-바닷속-수학.jpg)
![보트처럼 전진하는 나뭇잎 배 실험하기 [#핫클립]](/jnrepo/uploads/2021/11/보트처럼-전진하는-나뭇잎-배-실험하기-핫.jpg)
![[사이언스타임즈] 사물인터넷 가속화 이끈다](/jnrepo/uploads/2019/01/191176_web.jpg)

















